近日,從中國農業(yè)科學院
北京畜牧獸醫(yī)研究所獲悉,該所豬基因工程與種質創(chuàng)新團隊在國際上首次開展長達23個月的高脂高糖飲食飼喂小型豬研究,獲得了代謝綜合征模型,揭示了能量供應方式從葡萄糖轉變到酮體是觸發(fā)早期非酒精性脂肪性肝炎發(fā)生的關鍵事件。該研究成果于9月11日在線發(fā)表于國際刊物《科學報告(Scientific Reports)》雜志上。
據(jù)悉,脂肪肝等代謝性疾病嚴重危害人類健康。非酒精性脂肪肝病流行病學調查顯示,目前西方發(fā)達國家的患病率為20%-33%,我國患病率為12%-15%,患病人數(shù)達到1.5億~2.0億,并且逐年增加。早期脂肪肝極少受到重視,人類非酒精性脂肪性肝臨床材料嚴重匱乏,其發(fā)生機制研究一直空白。
牧醫(yī)所副研究員楊述林介紹,小型豬在飲食結構、營養(yǎng)代謝和解剖組織學等方面與人高度相似,因而成為開發(fā)人類代謝性疾病模型的適宜動物。為了揭示發(fā)生機制,
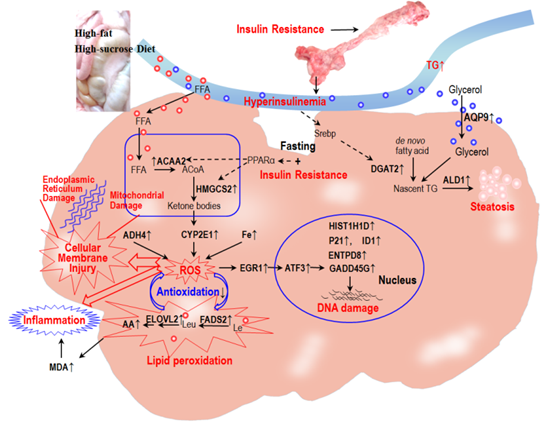
牧醫(yī)所豬基因工程與種質創(chuàng)新團隊與中國農業(yè)大學、上海交通大學醫(yī)學院附屬新華醫(yī)院、安徽醫(yī)科大學等單位合作,經過長期的高脂高糖飲食,小型豬表現(xiàn)出肥胖、高胰島素血癥、甘油三酯和低密度脂蛋白膽固醇持續(xù)升高,高密度脂蛋白膽固醇經過升高后轉為顯著降低與人代謝綜合征相似的病理特征。綜合肝臟成分、病理組織學和肝臟基因表達譜等數(shù)據(jù),該團隊科研人員揭示了非酒精性脂肪性肝炎早期發(fā)生的機制:(1)長期高脂高能量飲食促進體內脂肪大量沉積,引起胰島素抵抗和胰島代償性增殖,產生高胰島素血癥;(2)高胰島素促進肝臟內脂肪酸和甘油三酯的新生,并以脂微滴的形式彌散性沉積于肝細胞;(3)胰島素抵抗形成機體葡萄糖供應相對不足,肝臟將脂肪酸轉化成為大腦等關鍵器官供能的酮體;(4)肝臟高濃度酮體誘發(fā)細胞色素P450 2E1 (CYP2E1) 過表達;(5)CYP2E1和乙醇脫氫酶4過表達,以及鐵過載,促使活性氧(ROS)產生,損傷細胞內線粒體等膜結構;(6)ROS過氧化花生四烯酸和亞油酸等多不飽和脂肪酸,產生丙二醛誘發(fā)肝臟炎性反應;(7)ROS同時活化EGR1-ATF3-GADD45G信號通路,導致細胞核內DNA損傷。
據(jù)了解,
牧醫(yī)所近年來在小型豬糖脂代謝模型方面取得了引人注目的系列研究成果。先后成功獲得豬糖脂代謝誘導模型、心血管疾病轉基因豬模型、轉雙基因和三基因糖尿病豬模型。相關成果先后發(fā)表在國際知名刊物《胰腺(Pancreas)》、《公共科學圖書館·綜合(PLOS ONE)》、《分子醫(yī)學報告(Molecular Medicine Reports)》等雜志上,其中2014年11月發(fā)表在《公共科學圖書館·綜合(PloS One)》的“非酒精性脂肪性肝炎炎性細胞浸潤分子機制”一文被加拿大醫(yī)藥研究資訊公司—環(huán)球醫(yī)藥選為“關鍵科學文章”。該所獲得相關授權專利5項。先后獲國家973、863、國家自然科學基金等項目資助。
研究成果在線發(fā)表文章鏈接:
http://www.nature.com/articles/srep13980